
抗肿瘤免疫大腕,斯坦福大学的Irving Weissman教授课题组在正在举行的CRI-CIMT-EATI-AACR国际肿瘤免疫大会上报道了一种靶向PD-L1免疫哨卡的工程蛋白。这种工程蛋白分子量虽然较小,只有普通抗体的十分之一,但和PD-L1的亲和力却是PD-1的5万倍。临床前实验证明,这种PD-L1的蛋白拮抗剂不仅比传统的抗PD-1/PD-L1抗体的抗肿瘤疗效更好,而且和其它免疫疗法联合使用表现更好的的协同效应。这些初步临床前结果虽然说明这类新型的PD-L1的蛋白拮抗剂具有抗PD-1/PD-L1抗体的基本属性,但能取代抗PD-1/PD-L1抗体成为新一代的抗肿瘤免疫药物吗?
我们之前多次讨论,抗肿瘤免疫疗法是当下制药工业最热门的研究领域。不仅抗CTLA4抗体Yervoy、抗PD-1抗体Opdivo和Keytruda相继上市,还创造了多个“传奇”:比如默克Keytruda的“奇兵突起”超过施贵宝Opdivo,成为第一个登陆美国市场的PD-1抑制剂;FDA从接受申请到批准Opdivo的鳞状非小细胞肺癌适应症只用了短短4个工作日,创FDA审批记录;Opdivo三次因和标准疗法相比显示生存期优势其临床试验被提前终止等。PD-1抑制剂不仅在美国获批治疗晚期黑色素瘤、鳞癌非小细胞肺癌,在包括肾癌、膀胱癌、头颈癌、和三阴性乳腺癌等其它多个实体瘤和几个血癌适应症中也观察到疗效。免疫哨卡抑制剂的市场总额预计高达350亿美元。
虽然制药工业已经开发了许多抗PD-1、PD-L1、和CTLA4等免疫哨卡的单克隆抗体,其中包括百济神州的BGB-A317和江苏恒瑞的SHR-1210,但这些抗体作为单药使用的应答率还较低,平均只有15-20%。我们还不知道这些免疫哨卡抑制剂为什么应答率还比较低,但这些单克隆抗体具有一些比如分子量很大(大约150kDa),很难渗透到大一点的固体肿瘤等天生缺陷。除此之外,这些抗PD-1、PD-L1抗体一方面抑制免疫哨卡,提高免疫系统识别并清除肿瘤的功能,但同时也降低了PD-1、PD-L1起关键作用的杀伤肿瘤的免疫细胞,限制了这些抗体药物的治疗潜力。
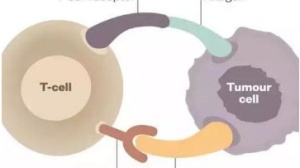
Weissman课题组通过一个称为“定向进化”(directed revolution)的开发平台设计了一种能靶向PD-L1,抑制PD-1/PD-L1信号传导的一种工程蛋白。这种工程蛋白既保持了传统PD-1/PD-L1抑制剂的生物功能,又不会消耗PD-1或PD-L1,导致以上所述的“误伤反作用”。其中最好的工程蛋白对PD-L1的亲和力比PD-1高5万倍,而其分子量只有普通抗体的十分之一大小。而且这个工程蛋白因为分子量小,正如预期的那样对肿瘤的浸润能力要明显优于抗体。比如研究人员通过荧光标记发现,这类蛋白能浸润到固体肿瘤的内部,而抗PD-1抗体主要存留在离肿瘤血管较近的区域。另一个更重要的优势是这些工程抗体不象抗PD-1、PD-L1抗体那样降低淋巴结T细胞的数目,不会“误伤” PD-1或PD-L1的其它免疫功能。
当然,这些靶向PD-L1的工程蛋白距上市并成为新一代的免疫疗法还有很长的路要走,比如因为这些工程蛋白分子比较小,更容易从体内排出,半衰期比较短,不能象抗体药物那样每2周甚至每月一次给药。这些工程蛋白也具有“免疫原性”,导致免疫系统对这些蛋白产生免疫反应。当然科学在迅速发展,今天在《自然》发表的“仿生纳米粒”或许就能解决其中的一些问题。
(来源:中美药源)
本文仅供医学药学专业人士阅读





.jpg-pd13)
.jpg-pd13)














 X
X