2015年9月,洛克菲勒大学的Rony Dahan等研究人员,在Cancer cell杂志上发表了一篇关于Fcγ受体影响PD-1,PD-L1抗体抗肿瘤活性的文章,该研究显示Fcγ受体的参与可以增强PD-L1抗体的抗肿瘤活性,但是Fcγ受体的参与也可以降低PD-1抗体的抗肿瘤活性。这些研究结果表明对抗体的Fc段进行更为合理的设计可以使得抗体的抗肿瘤活性达到最优。
最初,一些免疫调节性的抗体设计侧重于抗体的Fab段,然而,最近的研究发现抗体Fc端与I型Fcγ受体(FcγRI)之间的相互作用对于这些免疫调节性抗体介导的体内活性发挥重要作用。I型FcγR按功能分为两类:一类是激活性FcγR,小鼠体内主要包括FcγRI,FcγRIII和FcγRIV,而人主要是FcγRIA,FcγRIIA,FcγRIIIA;第二类是抑制性FcγR,FcγRIIB(包括小鼠和人)。激活性FcγR的生物学功能是由胞内的 ITAMs(immunoreceptor tyrosine-based activation motifs)调控,抗体Fc端与激活性FcγR结合后,通过胞内ITAMs促进细胞激活,内吞作用,吞噬作用。而抑制性FcγR通过胞内ITIMs(immunoreceptortyrosine-based inhibitory motifs)抑制细胞激活,内吞作用,吞噬作用。而对于一些抗肿瘤的抗体药物,抗体Fc端与激活性/抑制性的FcγRI结合后,会激活/抑制细胞吞噬作用,从而会引起肿瘤毒性,这种肿瘤毒性是由抗体依赖的细胞毒性(ADCC,Antibody-dependent cellular cytotoxicity)介导引起的,ADCC主要是通过NK细胞,巨噬细胞等表达I型FcγR效应细胞执行。所以,抗体的Fc端选择对于抗体体内抗肿瘤活性有非常重要的影响。为了检测不同的抗体Fc端对抗体体内抗肿瘤活性的影响,研究者通过对已有的PD-1,PD-L1的抗体进行改造,换上不同抗体亚型的Fc端,IgG1,IgG2α,IgG1-D265A(突变体,突变后不和任何FcR结合),对MC38结肠腺癌的小鼠注射治疗,结果显示Fc端为IgG2α的PD-L1抗体抗肿瘤活性最好,而Fc端不与FcR结合的PD-1抗体抗肿瘤活性最好。
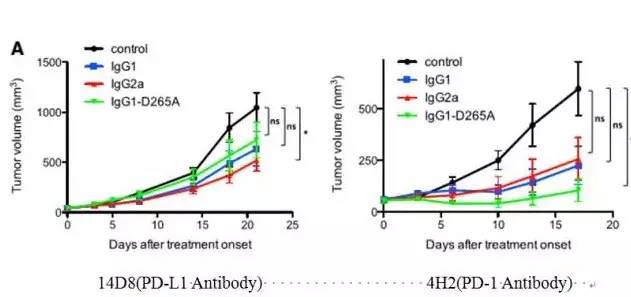 图1 嵌合PD-1/PD-L1抗体体内抗肿瘤活性
图1 嵌合PD-1/PD-L1抗体体内抗肿瘤活性
为了进一步探讨FcR的参与如何影响PD-L1抗体的体内抗肿瘤活性,研究人员制备了基因敲除小鼠,Fcer1g-/-(敲除激活性的FcγRs),治疗后结果显示,在敲除激活性的FcγRs的小鼠上,Fc端为IgG2α的抗体抗肿瘤活性显著降低(图2)。通过进一步的检测TME(肿瘤微环境)和脾脏的髓系来源的细胞,结果发现,在敲除小鼠TME里CD11b+F4/80+细胞比例显著下降,而其他两种MDSC(髓系来源抑制细胞)细胞没有显著变化(图3)。这些结果显示,激活性FcγRs的参与通过ADCC减少小鼠TME里CD11b+F4/80+细胞比例,从而提高亚型为IgG2α的PD-1抗体的活性。
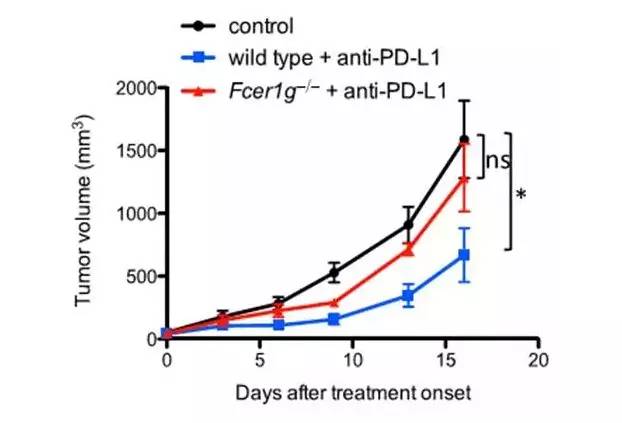 图2 嵌合PD-L1抗体体内抗肿瘤活性
图2 嵌合PD-L1抗体体内抗肿瘤活性
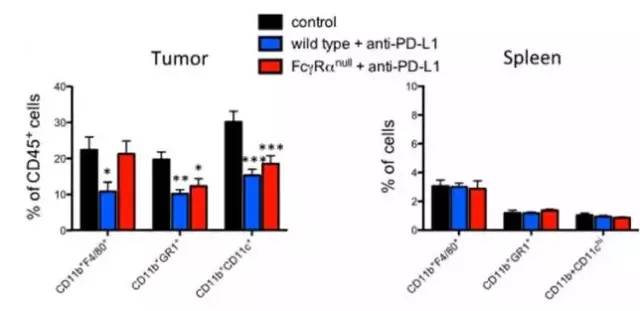 图3 TME和脾脏三种MDSC细胞比例的变化
图3 TME和脾脏三种MDSC细胞比例的变化
为了进一步探讨FcR的参与如何影响PD-1抗体的体内抗肿瘤活性,研究人员制备了基因敲除小鼠,Fcer1g-/-(敲除激活性的FcγRs),Fcer2b-/-(敲除抑制性的FcγRs)和Fcer1-/-(敲除FcγRI)。治疗后结果显示,敲除Fcer1g-/-或者Fcer1-/-后,PD-1抗体4H2(IgG2α)的抗肿瘤活性最佳。通过检测TME和脾脏的CD8+T细胞,CD4+T细胞和CD4+Treg细胞,结果发现,在敲除Fcer1g-/-或Fcer1-/-的小鼠TME里CD8+ T细胞显著提高,而其他两种细胞没有显著变化(图5)。这些结果显示,激活性FcγRs(主要是FcγRI)的参与通过ADCC减少CD8 TILs降低亚型为IgG2α的PD-1抗体的活性。
图4 嵌合的PD-1抗体的体内抗肿瘤活性
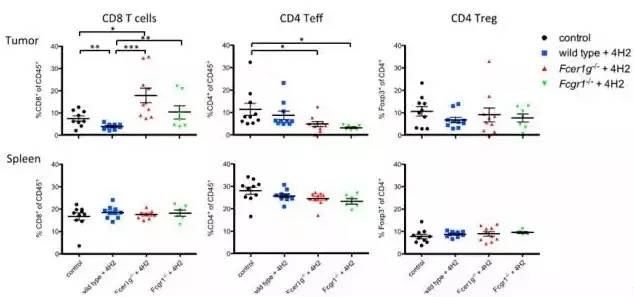
图5 激活性FcγRs的参与通过减少CD8 TILs降低PD-1抗体的活性
研究的结果充分显示对抗体的Fc段进行更为合理的设计可以使得抗体的抗肿瘤活性达到最优。
(来源:源正细胞)
本文仅供医学药学专业人士阅读
















 X
X