- 针对表皮生长因子受体-2(HER-2)的靶向药:曲妥珠单抗,帕妥珠单抗,T-DM1,拉帕替尼,来那替尼;
- PI3K/AKT/mTOR 通路抑制剂:依维莫司;
- 抗血管生成药物:贝伐珠单抗;
- 针对BRCA1/2突变的PARP抑制剂奥拉帕尼;
- CDK4/6抑制剂帕博西林。
HER-2靶向药
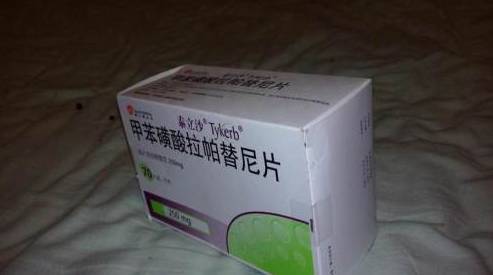 拉帕替尼治疗HER-2阳性且既往使用蒽环类、紫杉类和曲妥珠单抗治疗失败的晚期乳腺癌患者十分有效。
拉帕替尼是可以阻断EGFR和HER-2的双靶向药物。与曲妥珠单抗作用机制上不同的是,曲妥珠单抗只能阻断EGFR的胞外部分,而拉帕替尼可以阻断位于细胞内的截短型受体,解决了曲妥珠单抗治疗失败后再使用拉帕替尼交叉抗药的问题。
而且对于曲妥珠单抗治疗失败的HER-2阳性晚期乳腺癌患者,研究发现,拉帕替尼联合曲妥珠单抗与单药曲妥珠单抗维持相比,也能延长患者的总生存期(OS):60.7周 VS 41.4周。
绝经后HR阳性、HER-2阳性转移性乳腺癌的一线治疗,拉帕替尼联合来曲唑能得到更长的无进展生存期(PFS),219例给予拉帕替尼联合或不联合来曲唑的研究证实,联合组的中位PFS明显延长:8.2个月 VS 3.0个月。
拉帕替尼治疗复发或难治性炎性乳腺癌的Ⅱ期临床研究显示,126例HER-2阳性患者的有效率(ORR)为39%,对拉帕替尼有反应者的中位OS为18.4个月,无反应者为8.4个月。
拉帕替尼可穿透血-脑屏障而用于治疗乳腺癌脑转移。一项拉帕替尼治疗HER-2阳性乳腺癌伴新的或进展的脑转移瘤,但未经曲妥珠单抗治疗的Ⅱ期临床研究判读,242例患者中,6%达到部分缓解(PR)即达到最好的中枢神经系统(CNS)反应,21%有可测量病变的患者达到PR。而在拉帕替尼联合卡培他滨组,40%患者CNS肿瘤缩小≥20%。
3:帕妥珠单抗
拉帕替尼治疗HER-2阳性且既往使用蒽环类、紫杉类和曲妥珠单抗治疗失败的晚期乳腺癌患者十分有效。
拉帕替尼是可以阻断EGFR和HER-2的双靶向药物。与曲妥珠单抗作用机制上不同的是,曲妥珠单抗只能阻断EGFR的胞外部分,而拉帕替尼可以阻断位于细胞内的截短型受体,解决了曲妥珠单抗治疗失败后再使用拉帕替尼交叉抗药的问题。
而且对于曲妥珠单抗治疗失败的HER-2阳性晚期乳腺癌患者,研究发现,拉帕替尼联合曲妥珠单抗与单药曲妥珠单抗维持相比,也能延长患者的总生存期(OS):60.7周 VS 41.4周。
绝经后HR阳性、HER-2阳性转移性乳腺癌的一线治疗,拉帕替尼联合来曲唑能得到更长的无进展生存期(PFS),219例给予拉帕替尼联合或不联合来曲唑的研究证实,联合组的中位PFS明显延长:8.2个月 VS 3.0个月。
拉帕替尼治疗复发或难治性炎性乳腺癌的Ⅱ期临床研究显示,126例HER-2阳性患者的有效率(ORR)为39%,对拉帕替尼有反应者的中位OS为18.4个月,无反应者为8.4个月。
拉帕替尼可穿透血-脑屏障而用于治疗乳腺癌脑转移。一项拉帕替尼治疗HER-2阳性乳腺癌伴新的或进展的脑转移瘤,但未经曲妥珠单抗治疗的Ⅱ期临床研究判读,242例患者中,6%达到部分缓解(PR)即达到最好的中枢神经系统(CNS)反应,21%有可测量病变的患者达到PR。而在拉帕替尼联合卡培他滨组,40%患者CNS肿瘤缩小≥20%。
3:帕妥珠单抗
VEGF靶向药
mTOR靶向药 大家可以关注公众号”三阴姐妹互助圈“下载三阴乳腺癌的治疗资料包和添加病友群,请扫下面的二维码。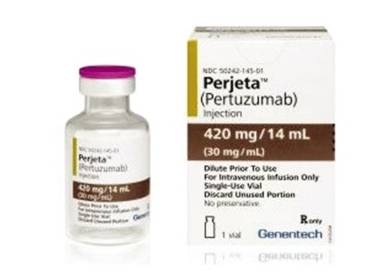 帕妥珠单抗为完全重组人源性单克隆抗体,与HER-2受体结合后在空间上阻碍其与EGFR、HER-3和HER-4的二聚化,从而阻断细胞内信号传导。
在CLEOPATRA试验中,在曲妥珠单抗联合多西他赛中加入帕妥珠单抗后,将中位总生存期从40.8个月提高到56.5个月。
2012年6月,美国FDA批准帕妥珠单抗用于转移性HER-2阳性乳腺癌的一线治疗。
曲妥珠单抗治疗失败的HER-2阳性晚期乳腺癌的ORR为24.2%,临床获益率为50%,中位PFS为5.5个月,总体来说耐受性良好。
4:来那替尼
来那替尼是一种口服的不可逆的EGFR酪氨酸激酶抑制剂,其作用靶点包括HER-1、HER-2和HER-4的细胞内酪氨酸激酶区。
Harold J等对136例HER-2阳性晚期乳腺癌患者的研究显示,无论既往治疗中是否使用过曲妥珠单抗,来那替尼的使用均可以获得较高的有效率。其中,对于曾经使用过曲妥珠单抗的患者,其ORR达24%;对于既往治疗中未使用过曲妥珠单抗的患者,ORR为56%。
国际多中心201试验部分结果显示,多线治疗后单药来那替尼有效率仍然高达61.5%(16/26)。而来那替尼联合曲妥珠单抗(202试验)对于曲妥珠单抗耐药患者仍然显示出一定疗效35%(7/20),主要不良反应为腹泻。
5:T-DM1
T-DM1是一种融合了抗体和细胞毒药物作用的新型靶向药物。Ⅱ期临床试验结果表明,T-DM1单药治疗已经接受过蒽环类、紫杉类、曲妥珠单抗和拉帕替尼治疗的转移性乳腺癌患者,有效率达到30%。
2012年,Ⅲ期的EMILIA研究纳入了978例既往接受曲妥珠单抗和紫衫烷类药物治疗的HER-2阳性转移性乳腺癌女性患者。在中位无进展生存期方面,T-DM1组为9.6个月,卡培他滨联合拉帕替尼组为6.4个月(P<0.0001)。证明了T-DM1比卡培他滨联合拉帕替尼效果更优。
帕妥珠单抗为完全重组人源性单克隆抗体,与HER-2受体结合后在空间上阻碍其与EGFR、HER-3和HER-4的二聚化,从而阻断细胞内信号传导。
在CLEOPATRA试验中,在曲妥珠单抗联合多西他赛中加入帕妥珠单抗后,将中位总生存期从40.8个月提高到56.5个月。
2012年6月,美国FDA批准帕妥珠单抗用于转移性HER-2阳性乳腺癌的一线治疗。
曲妥珠单抗治疗失败的HER-2阳性晚期乳腺癌的ORR为24.2%,临床获益率为50%,中位PFS为5.5个月,总体来说耐受性良好。
4:来那替尼
来那替尼是一种口服的不可逆的EGFR酪氨酸激酶抑制剂,其作用靶点包括HER-1、HER-2和HER-4的细胞内酪氨酸激酶区。
Harold J等对136例HER-2阳性晚期乳腺癌患者的研究显示,无论既往治疗中是否使用过曲妥珠单抗,来那替尼的使用均可以获得较高的有效率。其中,对于曾经使用过曲妥珠单抗的患者,其ORR达24%;对于既往治疗中未使用过曲妥珠单抗的患者,ORR为56%。
国际多中心201试验部分结果显示,多线治疗后单药来那替尼有效率仍然高达61.5%(16/26)。而来那替尼联合曲妥珠单抗(202试验)对于曲妥珠单抗耐药患者仍然显示出一定疗效35%(7/20),主要不良反应为腹泻。
5:T-DM1
T-DM1是一种融合了抗体和细胞毒药物作用的新型靶向药物。Ⅱ期临床试验结果表明,T-DM1单药治疗已经接受过蒽环类、紫杉类、曲妥珠单抗和拉帕替尼治疗的转移性乳腺癌患者,有效率达到30%。
2012年,Ⅲ期的EMILIA研究纳入了978例既往接受曲妥珠单抗和紫衫烷类药物治疗的HER-2阳性转移性乳腺癌女性患者。在中位无进展生存期方面,T-DM1组为9.6个月,卡培他滨联合拉帕替尼组为6.4个月(P<0.0001)。证明了T-DM1比卡培他滨联合拉帕替尼效果更优。

PARP靶向药
CDK4/6靶向药
咚咚总结
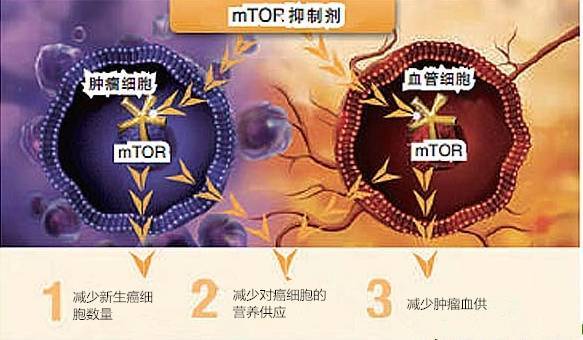 mTOR活性调控相当复杂,受多种调节信号蛋白的影响,其中主要受到两条信号通路调节,即PI3K/Akt/mTOR信号通路和LKB1/AMPK/mTOR信号通路。mTOR调节细胞的生存、增殖和细胞凋亡等细胞重要生理功能。因此,mTOR分子成为研究抗癌药物的靶向治疗上一个理想的目标。
依维莫司是首个获批用于治疗激素受体阳性/HER-2阴性乳腺癌的mTOR抑制剂。
第33届圣安东尼奥乳癌研讨会(SABCS)上公布了TAMRAD研究的结果,该研究主要评估了他莫昔芬/依维莫司对芳香酶抑制剂预治疗的激素受体阳性HER-2阴性乳腺癌妇女的疗效,中位随访时间为22个月。他莫昔芬组57名妇女的中位进展时间为4.5个月,联合用药组的54名妇女为8.6个月,疾病进展风险相对减少了47%(P=0.0026)。约80%的联合治疗组妇女30个月后仍旧存活,单用他莫昔芬组为40%左右,死亡相对危险度降低率为68%(P=0.0019)。
2015年ASCO年会上,美国学者对预测依维莫司疗效的指标进行了报道,发现常见的基因突变包括FGFR家族,PI3K/mTOR信号通路和TP53。基于这些基因的PFS无联性分析表明,PIK3CA突变或者PTEN无表达或低表达的患者可从依维莫司联合曲妥珠单抗联合化疗中获益。
mTOR活性调控相当复杂,受多种调节信号蛋白的影响,其中主要受到两条信号通路调节,即PI3K/Akt/mTOR信号通路和LKB1/AMPK/mTOR信号通路。mTOR调节细胞的生存、增殖和细胞凋亡等细胞重要生理功能。因此,mTOR分子成为研究抗癌药物的靶向治疗上一个理想的目标。
依维莫司是首个获批用于治疗激素受体阳性/HER-2阴性乳腺癌的mTOR抑制剂。
第33届圣安东尼奥乳癌研讨会(SABCS)上公布了TAMRAD研究的结果,该研究主要评估了他莫昔芬/依维莫司对芳香酶抑制剂预治疗的激素受体阳性HER-2阴性乳腺癌妇女的疗效,中位随访时间为22个月。他莫昔芬组57名妇女的中位进展时间为4.5个月,联合用药组的54名妇女为8.6个月,疾病进展风险相对减少了47%(P=0.0026)。约80%的联合治疗组妇女30个月后仍旧存活,单用他莫昔芬组为40%左右,死亡相对危险度降低率为68%(P=0.0019)。
2015年ASCO年会上,美国学者对预测依维莫司疗效的指标进行了报道,发现常见的基因突变包括FGFR家族,PI3K/mTOR信号通路和TP53。基于这些基因的PFS无联性分析表明,PIK3CA突变或者PTEN无表达或低表达的患者可从依维莫司联合曲妥珠单抗联合化疗中获益。
本文仅供医学药学专业人士阅读










-scaled.jpg-pd13)






 X
X