医学的世界宽广无边,有时候也会让人觉得冷热不均,厚此薄彼。同样是癌症,肺癌的研究就是热到发烫,治疗最近几年更是日新月异,但一些凶险程度毫不逊色的癌症,进步却是步履维艰。
比如说,属于消化系统癌症之一的食管癌。大家都知道,但凡跟消化系统沾边的癌症,几乎都不是善茬。肝癌、胃癌就都是中国多发,生存率也很低的癌症。而作为消化道上的第一关,食管癌虽说名气小一点,但治疗起来也是相当棘手的。
尤其是晚期食管癌患者,目前的5年生存率在5%的水平停滞不前,长期生存的患者屈指可数。相比之下,同样致命的肺癌,在免疫治疗时代,晚期患者的5年生存率已经达到了16%左右,相比过去4%的5年生存率,提高了足足四倍。
5年生存率停滞不前,就反映出了晚期食管癌治疗进步的缓慢。这种狠毒又难以对付的敌人,当然就得让道高一丈的免疫治疗来降服,但首先要了解的是,这魔高一尺的食管癌,到底凶险在什么地方。
▌“不能吃”和“吃出来”
现在有不少癌症患者,会用短视频的方式,记录自己的抗癌历程来鼓励自己,警示他人。实话说,有点不愿去看晚期食管癌患者的记录,因为他们往往被癌症剥夺了进食的能力。

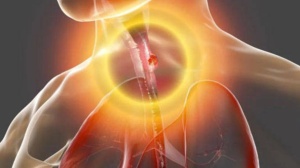
“咽喉要道”,在消化道中指的其实是食管才对
(图片来源:National Cancer Institute)
看上面这张图,应该就能明白食管里多了个肿瘤的影响有多可怕。民以食为天,晚期食管癌患者面对不能进食的痛苦,怎么谈得上有质量、有尊严地度过生命最后的时光呢?
但是有果必有因,食管癌本身,很大程度上也是一种吃出来的疾病,吃烫食、含亚硝酸盐多的腌制食物、以及霉菌过多的霉变食品,再加上抽烟喝酒,个个都算得上是病从口入了。
新中国食管癌防治工作的重点,就是从这些不良饮食习惯入手,在部分高发地区取得了初步的防治成功,比如著名的河南林县,食管癌的发病率就显著下降[1]。
防治+筛查,再配合对早期患者内镜治疗的进步,让中国食管癌的发病率和死亡率,近年来都有一定的下降[2]。不过到2012年,中国每年新发的食管癌接近30万例,死亡患者超过21万,仍然占到全世界的50%以上。

防治的成果还是整体向好的
(图片来源:Cancer Biology & Medicine)
防治癌症,最好是防和治一起进步,但防治+筛查主要针对的是早期食管癌患者,而晚期患者必须得在治上有进步,预后才能改善。目前即使算上早期患者,中国食管癌患者整体5年生存率也不足20%,这很大程度是被晚期患者的数据拉低的。
不过治疗要进步,还得考虑到食管癌有东西方迥异的特点,中国患者组织学类型以鳞癌为主,与欧美国家的腺癌为主差异很大,所以一些欧美国家使用的治疗方案,在中国不见得会合适。
目前,医生们主要又是用什么手段,挑战凶恶的食管癌呢?
▌进步缓慢,还是方兴未艾?
手术刀,可以说是人类对抗癌症最古老的武器,外科手术也是很多人眼中根治癌症的唯一希望。但食管所在的“咽喉要道”,实在是人体的要害之处,手术的风险绝对不能忽视。
即使是到了21世纪,在手术量大、手术经验丰富的医院,食管癌外科手术的围术期死亡率也仍然有5%左右[3]。而且与所有的癌症类似,至少一半的食管癌患者,在确诊时就已经不适合手术为主的多学科治疗了[4]。
手术没条件做,那大家第一时间肯定都会想到放化疗,但对于不能手术的局部晚期或转移性食管癌患者,放化疗的获益,就远远比不上配合手术时的效果了。

消化道癌症普遍都不吃放化疗这一套
(图片来源:Pixabay)
目前临床指南推荐的晚期患者化疗,基本上一线是以氟尿嘧啶+铂类药物为主,但不管是双药还是三药联合,疗效都比较局限,患者的生存期也就是8-10个月。
一线化疗效果不好,二线的单药化疗就更是可想而知了,不仅疗效数据不算好,客观缓解率(ORR)只有3-6%,而且很多药物使用的证据,都还是来自规模较小的II期试验。
至于靶向治疗,目前适用的群体很有限。一线治疗有靶向HER2的曲妥珠单抗,但只适用于大约20%的食管腺癌患者,二线治疗的抗血管生成药物雷莫芦单抗也限于腺癌。对中国占比例接近90%的鳞癌患者来说,这些疗法的价值就很难讲了。
癌症基因组图谱计划(TCGA)也显示,食管鳞癌和食管腺癌特性迥异,大多数常见的基因突变,都还暂时“不可成药”(Undrugable),靶向治疗进步慢也是无奈的事[5]。

食管腺癌可能会分出许多亚型,但食管鳞癌暂时还不能细分
(图片来源:Nature)
面对这样的困局,只能大喊一声“有心杀贼,无力回天”了。而攻克这座雄关的强手,正是打遍十八路癌症的免疫治疗。
2019年7月,PD-1抑制剂帕博利珠单抗(Pembrolizumab)获得FDA的批准,用于接受过一线治疗后病情进展,且PD-L1阳性(CPS≥10)的复发性、局部晚期或转移性食管鳞状细胞癌(ESCC)患者。
这次获批,标志着食管癌正式进入了免疫治疗时代。对于在痛苦中挣扎的中国食管癌患者来说,能有免疫治疗这个全新的选择,当然是再好不过。
而且免疫治疗这位当红炸子鸡不来则已,一来就是“三国演义”。在帕博利珠单抗获批之后,同是PD-1抑制剂的纳武利尤单抗(Nivolumab)和卡瑞利珠单抗(Camrelizumab),也相继宣布了食管癌二线治疗的临床III期试验成功。
这三强在试验中的表现,就很值得细品一番了。
▌三英战吕布
帕博利珠单抗是三强中适应证最多的一个,又最先获批食管癌适应证,那就从它获批的主要依据——临床III期试验KEYNOTE-181说起吧。
其实KEYNOTE-181试验,是一项入组患者情况复杂,终点也有好几项的试验,它同时考量了帕博利珠单抗对食管腺癌、胃食管连接部腺癌,以及获批适应症对应的PD-L1阳性(CPS≥10)、“治疗有限”的食管鳞癌患者的治疗价值。
复杂性还不止入组患者这一点。比如与帕博利珠单抗治疗组对比的对照组,单药化疗就可以从紫杉醇、多西他赛和伊立替康当中任选一种;又比如试验的主要终点总体生存期(OS),要依次在PD-L1阳性患者、鳞癌患者和患者整体中检验。

说着好绕,看图吧
(图片来源:2019 ASCO GI)
从试验数据来看,帕博利珠单抗的OS获益,主要体现在试验中的PD-L1阳性患者组,患者的OS从6.7个月提高到9.3个月,死亡风险相对下降了31%(HR 0.69)。

这三分之一患者的获益趋势很明显
(图片来源:2019 ASCO GI)
2019年的欧洲肿瘤内科学会(ESMO)上,公布的KEYNOTE-181试验中国患者数据显示,PD-L1阳性的中国食管鳞癌患者,OS从化疗的5.3个月提高到了12个月,死亡风险相对降低了66%,12个月生存率从16%提升到53%[6]!
换句话说,相比起KEYNOTE-181患者整体,帕博利珠单抗单药治疗中国食管癌患者的获益幅度更大,尤其是12个月生存率的显著提升,对过去的晚期食管癌治疗来说是几乎不可想象的。
用这项试验的中国牵头人,北京大学肿瘤医院沈琳教授的话说,“药物治疗能让食管癌患者的中位OS突破一年,都已经非常罕见了,更何况这还是一项二线治疗试验。帕博利珠单抗的这种获益,是食管癌治疗史上前所未见的提升”。
帕博利珠单抗的老对手纳武利尤单抗,最近凭借III期试验ATTRACTION-3的成功,不久前在日本获批用于食管鳞癌的治疗,但这项试验并未入组中国患者[7]。这种时候就只能通过东亚患者亚组,去间接推测中国患者获益了。

有些癌症上,中国患者也和亚洲其他地方差异明显
(图片来源:Pixabay)
三强中的卡瑞利珠单抗,则是最晚公布食管癌试验的数据。从疗效上看,卡瑞利珠单抗的成绩并不差,但试验中的不良事件相关数据却值得注意。
比化疗更安全,本来应该是免疫治疗的一大优势,但在卡瑞利珠单抗的ESCORT试验中,免疫治疗组的不良事件发生率却稍高于化疗组(94.3%对90%),尤其是反应性皮肤毛细血管增生症(RCCEP)的发生率达到79.8%[8]。
这一数据与此前卡瑞利珠单抗早期试验的安全性相似,不过整体而言,免疫治疗组3级以上不良事件发生率仍明显低于化疗(19.3%对39.5%),发生的RCCEP也主要以1-2级为主。至于RCCEP的成因和影响,还需要后续研究来进一步明确。
总而言之,免疫治疗的三强争霸,让晚期食管癌患者终于在有效率低、副作用大的化疗之外,看到了新的希望,别忘了,免疫治疗的有效,可是一旦实现缓解,就能长久获益啊。
据了解,帕博利珠单抗食管癌的适应证在中国已经处于审评审批中,获批在即,中国食管癌的患者也将多一个治疗选择。而三强争霸的下一个战场——晚期食管癌的一线治疗如果能早日取得突破,就再好不过啦。
参考资料:
1.Zeng H, Zheng R, Zhang S, et al. Esophageal cancer statistics in C hina, 2011: Estimates based on 177 cancer registries[J]. Thoracic Cancer, 2016, 7(2): 232-237.
2.Liang H, Fan J H, Qiao Y L. Epidemiology, etiology, and prevention of esophageal squamous cell carcinoma in China[J]. Cancer Biology & Medicine, 2017, 14(1): 33.
3.Allum W H, Bonavina L, Cassivi S D, et al. Surgical treatments for esophageal cancers[J]. Annals of the New York Academy of Sciences, 2014, 1325: 242.
4.Van Rossum P S N, Mohammad N H, Vleggaar F P, et al. Treatment for unresectable or metastatic oesophageal cancer: current evidence and trends[J]. Nature Reviews Gastroenterology & Hepatology, 2018, 15(4): 235.
5.Cancer Genome Atlas Research Network. Integrated genomic characterization of oesophageal carcinoma[J]. Nature, 2017, 541(7636): 169-175.
6.Chen J, Luo S, Qin S, et al. 760P Pembrolizumab vs chemotherapy in patients with advanced/metastatic adenocarcinoma (AC) or squamous cell carcinoma (SCC) of the esophagus as second-line therapy: Analysis of the Chinese subgroup in KEYNOTE-181[J]. Annals of Oncology, 2019, 30(Supplement_5): mdz247. 086.
7.Kato K, Cho B C, Takahashi M, et al. Nivolumab versus chemotherapy in patients with advanced oesophageal squamous cell carcinoma refractory or intolerant to previous chemotherapy (ATTRACTION-3): a multicentre, randomised, open-label, phase 3 trial[J]. The Lancet Oncology, 2019, 20(11): 1506-1517.
8. Huang J, Xu JM, Chen Y, Zhuang W, Zhang YP, Chen ZD, et al. Phase 3 study of camrelizumab vs chemotherapy for locally advanced/metastatic esophageal cancer: the ESCORT Study. In: Oral Presentation at the 15th OESO World Conference for Esophaeal Diseases (2019).
本文仅供医学药学专业人士阅读



















 X
X