要点提示
-
前沿:TIGIT+PD-L1单抗数据更新:一线治疗NSCLC,PD-L1高表达人群疾病进展或死亡风险降低71% -
新药:一线治疗鼻咽癌!百济神州PD-1单抗III期临床结果公布,已报上市 -
新药:一线治疗NSCLC,君实生物递交PD-1抑制剂新适应证上市申请 -
新药:一线食管癌、鳞状NSCLC,恒瑞卡瑞利珠单抗两项新适应证获批
01
前沿:TIGIT+PD-L1单抗数据更新:一线治疗NSCLC,PD-L1高表达人群疾病进展或死亡风险降低71%
结果显示,经过2.5年的中位随访期后,tiragolumab+阿替利珠单抗对意向治疗人群(ITT,n=67)持续显示有临床获益,使ITT人群的疾病恶化或死亡风险降低了38%[无进展生存期(PFS)=5.6 vs 3.9个月,HR=0.62,95% CI: 0.42-0.91],改善了客观缓解率(ORR)(38.8% vs 20.6%)。
在PD-L1高表达人群中预定的探索性分析结果显示,tiragolumab+阿替利珠单抗可使疾病进展或死亡风险降低71%(PFS=16.6 vs 4.1个月,HR=0.29,95% CI:0.15-0.53),ORR得到具有临床意义的显著改善(69.0% vs 24.1%)。
TIGIT+阿替利珠单抗 vs 阿替利珠单抗一线治疗PD-L1阳性转移性NSCLC的疗效和安全性
在次要终点方面,tiragolumab+阿替利珠单抗也使ITT人群的总生存期(OS)得到改善(23.2 vs 14.5个月,HR=0.69,95% CI: 0.44-1.07)。在针对PD-L1高表达人群的预定探索性分析中,tiragolumab+阿替利珠单抗组的OS也观察到了具有临床意义的显著改善(未成熟 vs 12.8个月),预计可超过30.3个月。
安全性方面,tiragolumab+阿替利珠单抗耐受性良好,与对照组药物的3-4级治疗相关不良事件的发生率相似(22.4% vs 25%),最常见(≥5%)的全因不良反应包括注射反应、强直、皮肤干燥、疲劳、红疹等。经过更长时间随访,未发现新的安全性事件。
02
新药:一线治疗鼻咽癌!百济神州PD-1单抗III期临床结果公布,已报上市
RATIONALE 309是一项随机、双盲、安慰剂对照的III期临床试验,旨在对比替雷利珠单抗联合吉西他滨和顺铂与安慰剂联合吉西他滨和顺铂作为复发或转移性鼻咽癌一线疗法的有效性和安全性。试验的主要终点是经独立评审委员会(IRC)对ITT人群评估的PFS;关键次要终点是:OS、经IRC评估的ORR和缓解持续时间(DoR),以及经研究者评估的PFS。
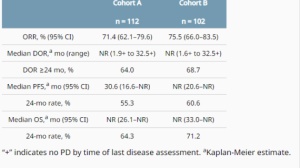
该研究共入组263名患者,分别有131例和132例患者随机分配至替雷利珠单抗组(A组)和安慰剂组(B组),两组患者的基线特征均衡。截至2021年3月26日,试验中位随访时间为10个月,结果如下:
根据IRC的评估,A组显著延长了患者的中位PFS(9.2月 vs 7.4月,p<0.0001,HR=0.52 95% CI:0.38-0.73] ),ORR更高[69.5% vs 55.3%;完全缓解(CR)率:16.0% vs 6.8%),中位DoR更长(8.5月 vs 6.1月)。A组第6、9和12个月的PFS率分别为66.1%、51.0%和35.7%,B组分别为53.0%、21.6%和12.2%。
根据研究者评估,A组中位PFS为9.8个月,B组为7.6个月(HR=0.54,95% CI:0.38-0.76)。在大多数患者亚组中观察到一致的PFS获益,无论患者疾病状态、基线肝转移指数和性别。
替雷利珠单抗联合化疗组表现出可控的安全性,与每种治疗药物的已知风险一致,未发现新的安全信号。
此前,5月21日,百济神州宣布,替雷利珠单抗联合化疗,对比安慰剂联合化疗,作为用于治疗复发或转移性鼻咽癌患者一线疗法的III期临床试验在中期分析中达到主要终点。基于此,国家药品监督管理局药品审评中心(CDE)已于2021年8月受理了该适应证的上市申请。
03
新药:一线治疗NSCLC,君实生物递交PD-1抑制剂新适应证上市申请
本次新适应证的上市申请基于CHOICE-01研究(NCT03856411),研究同时纳入了晚期鳞癌和非鳞癌NSCLC两种组织学类型患者,并将抗PD-1单抗联合化疗作为一线治疗的随机、双盲、安慰剂平行对照、多中心Ⅲ期临床研究,由中国医学科学院肿瘤医院王洁教授担任主要研究者。
该研究在全国63家中心共入组了465例NSCLC患者,其中鳞癌受试者220例,非鳞癌受试者245例,按照2:1随机入组,鳞癌受试者接受特瑞普利单抗/安慰剂联合白蛋白结合型紫杉醇+卡铂治疗,非鳞癌患者接受特瑞普利单抗/安慰剂联合培美曲塞+顺铂/卡铂治疗。疾病进展后,符合条件的对照组受试者可接受特瑞普利单抗单药的交叉治疗。
根据CHOICE-01研究的期中分析结果,独立数据监察委员会(IDMC)判定其主要研究终点PFS达到方案预设的优效界值。研究结果以口头汇报形式在2021年世界肺癌大会(WCLC)上公布。结果显示,与单纯化疗方案相比,特瑞普利单抗联合化疗一线治疗晚期NSCLC可显著延长患者的PFS,降低疾病进展风险,并在OS方面观察到了获益趋势。
04
新药:一线食管癌、鳞状NSCLC,恒瑞卡瑞利珠单抗两项新适应证获批
NMPA官网截图
2020年12月16日,卡瑞利珠单抗一线治疗鳞状NSCLC的III期临床研究(SHR-1210-III-307)和一线治疗晚期食管癌的III期临床研究(ESCORT-1st)主要研究终点结果达到方案预设的优效标准。
SHR-1210-III-307是一项随机、双盲、安慰剂对照的III期临床,旨在评估卡瑞利珠单抗或安慰剂联合紫杉醇和卡铂一线治疗晚期或转移性鳞状NSCLC有效性和安全性。主要研究终点是由盲态独立评审委员会(BIRC)根据RECIST v1.1标准评估的PFS,次要研究终点是OS、研究者评估的PFS、ORR和安全性等。
结果表明,卡瑞利珠单抗联合化疗用于晚期或转移性鳞状NSCLC患者一线治疗,可显著延长患者的PFS。
ESCORT-1st是一项随机、双盲、安慰剂对照的III期研究,旨在评估卡瑞利珠单抗联合紫杉醇和顺铂对比安慰剂联合紫杉醇和顺铂用于晚期食管癌一线治疗的有效性和安全性。主要终点是由IRC根据RECIST v1.1标准评估的PFS和OS,次要研究终点是研究者评估的PFS、ORR、DoR、疾病控制率(DCR)和安全性等。研究结果在四大顶级医学期刊之一的《美国医学会杂志》(JAMA,IF:56.272)上发表。
结果显示,与化疗相比,卡瑞利珠单抗联合化疗可显著延长患者的中位OS(15.3个月vs 12.0个月),降低30%的死亡风险,同时也显著延长患者的中位PFS(6.9个月vs 5.6个月),降低44%的疾病进展风险。卡瑞利珠单抗联合化疗组患者的ORR 更高(72.1% vs 62.1%),DoR更长(7.0个月 vs 4.6个月)。安全性方面,两组中≥3级治疗相关的不良反应事件发生率相当(63.4% vs 67.7%),其中常见的≥3级治疗相关的不良反应事件是中性粒细胞计数减少(39.9% vs 43.4%)。
[2]https://mp.weixin.qq.com/s/77pXrOWBeNcJHxNYOK35Gw [3]https://mp.weixin.qq.com/s/4LfqdhmfQaR1TStpwJBB-Q [4]https://mp.weixin.qq.com/s/OF-Eta-yncxvECMLRMHzMQ
本文仅供医学药学专业人士阅读


















 X
X