时隔49天,美国国家综合癌症网络NCCN于2021年8月16日悄然将乳腺癌临床实践指南更新至2021年第6版。本次更新内容不多,主要是根据KEYNOTE-522研究结果,新增了K药在早期高危三阴乳腺癌中的应用,让我们一起来学习一下吧~

新增高风险三阴乳腺癌推荐方案:
术前帕博利珠单抗联合化疗,
术后序贯帕博利珠单抗
高风险三阴性乳腺癌新增推荐方案:术前帕博利珠单抗+卡铂+紫杉醇 → 术前帕博利珠单抗+环磷酰胺+多柔比星或表柔比星 → 术后帕博利珠单抗。
新增脚注j:高风险标准包括II~III期三阴性乳腺癌。术后帕博利珠单抗(2A类证据)可个体化。
参考文献:Schmid P, Cortes J, Pusztai L, et al. Pembrolizumab for early triple-negative breast cancer. N Engl J Med, 2020;382(9):810-821

相关临床试验:
2021年7月27日,FDA正式批准帕博利珠单抗(Keytruda)用于治疗高危、早期三阴性乳腺癌(TNBC)患者,联合化疗作为新辅助治疗,然后继续作为单药作为手术后的辅助治疗。此次批准是基于一项名为KEYNOTE-522的III期临床试验结果。
在KEYNOTE-522试验中,所有入组的患者按 2:1 的比例随机接受每 3 周 200 毫克的K药(n = 784)或安慰剂(n = 390)。 所有患者都接受了 4 个周期的卡铂+紫杉醇治疗,以及 4 个周期的阿霉素或表柔比星+环磷酰胺。并且手术后治疗组的患者继续辅助K药治疗 9 个周期或直至疾病复发或出现不能耐受的毒性。无事件生存率(EFS)和病理完全缓解 (pCR) 是该研究的双重主要终点。
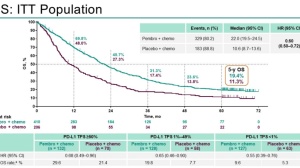
中位随访 39.0 个月后,与化疗/安慰剂方案相比,K药方案将疾病进展风险降低了 37%(HR,0.63;95% CI,0.48-0.82;P = .00031)。此外,与化疗/安慰剂方案相比,K药方案还将死亡风险降低了 28%(HR,0.72;95% CI,0.51-1.02;P = .03214),但是这一区别尚未达到统计显著水平,没有统计学意义。
在 2019 年 ESMO 大会期间提交的第一次中期分析数据表明,在接受K药治疗方案的患者中,有64.8% 的患者(n = 401)观察到了 pCR,而在单独接受化疗的患者中为 51.2%(n = 201;P = .00055)。且无论 pCR 定义如何,都能从K药免疫治疗方案中获益。
在 498 名 PD-L1 阳性患者(定义为综合阳性评分 (CPS) 为 1 或更高)的亚组中,K药研究组的 pCR 率为 68.9%,而安慰剂组为 54.9%,增加了 14 %(CI,5.3-23.1);在 97 名 PD-L1 阴性(定义为 CPS 小于 1)的患者中,研究组和对照组的 pCR 率分别为 45.3% 和 30.3%,增加了 15%(CI,-3.3 -36.8 )。3 年时,84.5% 接受K药联合化疗的患者存活并且没有发生 EFS 事件,而单独接受化疗的患者中有 76.8%。

图片来源:八卦小和尚(感谢分享!~)
此外,在预先指定的 EFS 探索性亚组分析中,发现K药治疗方案获得的益处与 PD-L1 的表达状态无关。在 973 名 PD-L1 阳性患者中,K药+化疗与单独化疗相比,将 EFS 风险降低了 33%(HR,0.67;95% CI,0.49-0.92)。在 197 名 PD-L1 阴性患者中,K药+化疗与单独化疗相比,将 EFS 事件的风险降低了 52%(HR,0.48;95% CI,0.28-0.85)。
大家可以关注公众号”三阴姐妹互助圈“下载三阴乳腺癌的治疗资料包和添加病友群,请扫下面的二维码。

在安全性方面,K药组中观察到≥3级与治疗相关的AE(TRAE)发生率为5.7%(vs 1.9%)。最常见的 TRAE 包括关节痛(7.9% vs 6.7%)、皮疹(4.9% vs 2.2%)和瘙痒(4.2% vs 2.2%)。
增加术前帕博利珠单抗+化疗
术后辅助帕博利珠单抗的剂量/给药细节
术前:第1天K药200毫克;第1、8、15天紫杉醇80毫克/m^2;第1天卡铂AUC5-每21天一个周期x4个周期(周期1-4)
然后:第1天K药200毫克;第1天阿霉素60毫克/m^2或阿柔霉素90毫克/m^2;第1天环磷酰胺600毫克/m^2-每21天一个周期x4个周期(周期5-8)
术后:第1天辅助帕博利珠单抗200毫克,每21天一个周期x9个周期

修改HER2阴性乳腺癌推荐方案:
奥拉帕利荣登NCCN指南推荐!
HER2阴性乳腺癌术前(新辅助)或(术后)辅助治疗推荐方案修改:如果种系(又称胚系、生殖系、可遗传)BRCA1和/或BRCA2突变,可以奥拉帕利。
修改脚注g:对于种系BRCA1/2突变伴(1)三阴性乳腺癌和病理肿瘤分期≥T2期或病理淋巴结分期≥N1期(1类证据)或(2)激素受体阳性且HER2阴性且淋巴结阳性≥4枚者,考虑辅助化疗后加奥拉帕利辅助治疗1年。对于种系BRCA1/2突变且激素受体阳性且HER2阴性乳腺癌术前化疗者,如果残留病变且临床和病理分期+雌激素受体状态和肿瘤分级(CPS+EG)评分≥3分,考虑奥拉帕利辅助治疗1年。术后奥拉帕利可与内分泌治疗同时用药。

相关临床试验:
在上一版(2021 V5)NCCN指南中,首次将奥拉帕利列入指南推荐。主要是根据2021 ASCO临床肿瘤学会上发表的OlympiA 3期研究结果。
OlympiA 研究是一项多中心、随机、安慰剂对照试验,共招募了 1836 例携带种系BRCA突变的HER2 阴性乳腺癌患者,他们以 1:1 的比例随机接受每天两次 300 mg 口服奥拉帕利(n = 921)为期 1 年或安慰剂治疗(n = 915)。此外,患者需要接受早期(II-III 期)乳腺癌的治疗,并完成手术和化疗,无论是否接受放疗。纳入标准还要求患者具有疾病高复发风险,而那些先前接受过 PARP 抑制剂治疗的人没有资格参加。

结果表明:在中位随访 2.5 年后,接受奥拉帕利治疗的患者减少了 42% iDFS(风险比 [HR]=0.58;99.5% CI=0.41-0.82;P <.0001 )。此外,研究人员们还注意到奥拉帕利和安慰剂之间的 3 年 iDFS 率差异为 8.8%(95% CI=4.5%-13.0%;分层HR=0.58;99.5% CI=0.41-0.82;P <.0001)。DDFS 降低了43%(HR=0.57;99.5% CI= 0.39-0.83;P <.0001),奥拉帕利和安慰剂的 3年DDFS率差异为 7.1%(95% CI=3.0%-11.1%;分层HR=0.57;99.5%=0.39-0.83;P <.0001)。
在中位随访 2.5 年时,接受奥拉帕尼与安慰剂的患者报告的死亡人数较少,两个研究队列之间的 OS 没有显著差异(HR=0.68;99% CI=0.44-1.05;P = .024);此外,两组之间的 3 年 OS 率差异为 3.7%(95% CI=0.3%-7.1%)。
就安全性而言,奥拉帕利组报告的不良反应 (AE) 与先前报告的结果一致。此外,奥拉帕利没有增加严重的 AE,包括住院或其他癌症(如白血病)的发生。
修改HER2阳性曲妥珠治疗方案:
每28天一个周期
每28天的第1、8、15天静脉注射多西他赛35mg/m²

本文仅供医学药学专业人士阅读



.jpg-pd13)

.jpg-pd13)





-scaled.jpg-pd13)






 X
X