要点提示
01
Nature:免疫+靶向+化疗,实现胃癌治疗新突破:KEYNOTE-811研究中期分析结果公布
研究发表截图
在该研究中,研究人员测试了PD-1抗体帕博利珠单抗联合曲妥珠单抗和化疗治疗HER2阳性胃癌的效果。研究纳入了434名晚期HER2阳性胃癌患者,217被分配到帕博利珠单抗组,接受帕博利珠单抗+曲妥珠单抗+化疗的治疗,216人被分配到安慰剂组,仅接受曲妥珠单抗+化疗的治疗。
此次中期分析时,全体患者中位随访了9.9个月。133名帕博利珠单抗组患者和131名安慰剂组患者被纳入了疗效分析,这些患者中位随访12.0个月。分析显示,帕博利珠单抗组和安慰剂组的客观缓解率(ORR)分别为74.4%和51.9%。在曲妥珠单抗+化疗的基础治疗方案中加入帕博利珠单抗,HER2阳性胃癌患者的ORR提高了22.7%。
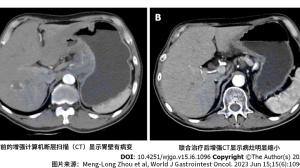
此外,帕博利珠单抗组患者的肿瘤缩小也更为明显。相比基线时,帕博利珠单抗组患者的肿瘤体积中位缩小了65%,而安慰剂组中位缩小了49%。32.3%的帕博利珠单抗组患者肿瘤缩小超80%,而只有14.8%的安慰剂组患者肿瘤缩小超80%。
在安全性方面,帕博利珠单抗组和安慰剂组的严重不良反应发生率相似,分别为57.1%和57.4%。两组中分别有24.4%和25.9%的患者因不良反应停止治疗,3.2%和4.6%的患者因不良反应死亡。两组中最常见的不良反应都是腹泻、恶心和贫血。
02 大家可以关注公众号”三阴姐妹互助圈“下载三阴乳腺癌的治疗资料包和添加病友群,请扫下面的二维码。 前沿:首款TROP2 ADC正式进入中国台湾!二线治疗TNBC患者ORR达38.8%
目前,美国食品药品监督管理局(FDA)已加速批准帕博利珠单抗联合曲妥珠单抗、氟嘧啶和含铂化疗药物用于局部晚期不可切除或转移性HER2阳性胃癌或胃食管交界腺癌患者的一线治疗。

戈沙妥珠单抗是一款抗TROP-2抗体药物偶联物(ADC)。由抗TROP-2单抗和细胞毒SN-38组成。2021年5月,中国国家药品监督管理局(NMPA)受理了戈沙妥珠单抗的生物制品上市许可申请(BLA),用于治疗接受过至少两种系统治疗(其中至少一种为针对转移性疾病的治疗)的不可切除的局部晚期或mTNBC成人患者,并被纳入优先审评品种。该申请目前正在审理中。
EVER-132-001是一项单臂、多中心的Ⅱb期注册研究,在中国招募的80例患者中评估戈沙妥珠单抗用于治疗既往接受过至少两种系统治疗(其中至少一种为针对转移性疾病的治疗)的不可切除的局部晚期或mTNBC成人患者的疗效。参与者在 21 天治疗周期的第1天和第8天以10mg/kg的剂量静脉注射戈沙妥珠单抗。治疗一直持续到疾病进展、出现不可接受的毒性或撤回同意。
研究结果显示经独立审评委员会(BIRC)评估的ORR为38.8%。此外,该药剂的毒性特征与之前检查其使用的其他临床试验中报告的毒性特征相当。没有观察到新的安全信号。
03 新药:泽布替尼获CDE拟突破性疗法,治疗成人CLL/SLL
CDE官网截图
泽布替尼是一款布鲁顿氏酪氨酸激酶(BTK)小分子抑制剂,目前正在全球进行广泛的临床试验项目,作为单药和与其他疗法进行联合用药治疗多种B细胞恶性肿瘤。由于新的BTK会在人体内不断合成,泽布替尼在设计上优化了生物利用度、半衰期和选择性,实现对BTK蛋白完全且持续的抑制。凭借与其他获批BTK抑制剂存在差异化的药代动力学,泽布替尼能在多个疾病相关组织中抑制恶性B细胞增殖。
在中国,泽布替尼已有3项适应证获NMPA附条件批准上市,分别是既往至少接受过一种治疗的成年套细胞淋巴瘤(MCL)患者、既往至少接受过一种治疗的成年CLL/SLL患者和既往至少接受过一种治疗的成年华氏巨球蛋白血症(WM)患者。值得注意的是,泽布替尼获批的3项适应证均已纳入国家医保药品目录。
04
新药:圣和药业PI3Kδ抑制剂获CDE拟突破性疗法,治疗滤泡性淋巴瘤
CDE官网截图
PI3K(磷酯酰肌醇-3-激酶)及其下游分子信号蛋白激酶B(Akt)/雷帕霉素靶蛋白(mTOR)所组成的信号通路是哺乳动物最重要的细胞内信号通路之一,对多种重要生理功能至关重要,包括细胞周期、细胞存活、蛋白质合成和生长、代谢、运动和血管生成,与众多血液瘤和实体瘤的发生有关。
SHC014748M是由圣和药业自主研发的PI3Kδ选择性抑制剂,能够选择性抑制PI3Kδ激酶活性,抑制下游通路信号转导,影响B细胞的生长、发育、成熟和分化,阻断B淋巴细胞肿瘤的发生发展。圣和药业正在开展SHC014748M治疗FL的II期临床试验。
[2] https://mp.weixin.qq.com/s/CXOvZQept-QO0ZzgBvvSqw
[3] https://mp.weixin.qq.com/s/bKq8pyoVsw97udUIK-y1Gw
[4] https://mp.weixin.qq.com/s/XJUPyH3Q-KTFkcUZsCe2Mg
本文仅供医学药学专业人士阅读

















 X
X