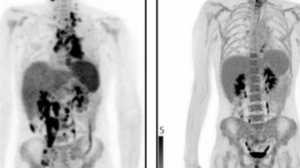
这是一位T细胞淋巴瘤患者的PET/CT影像。治疗前他的肿瘤已经遍布全身,而在治疗1个月后,肿瘤已经几乎完全消失,达到了完全缓解的标准。
这位患者参加的是一种CAR-T疗法WU-CART-007的I/II期临床试验,和他一样接受II期推荐方案治疗的11位患者,8人完全缓解,2人部分缓解,客观缓解率和完全缓解率分别达到了90.9%和72.7%[1]。
而且WU-CART-007是一种异体CAR-T疗法,不需要针对每位患者进行个性化制备,治疗成本相比现有的CAR-T疗法也将大幅降低。
CAR-T疗法已经成为治疗B细胞恶性肿瘤的一种主要方法,目前的CAR-T疗法几乎都需要使用患者自身的T细胞来制备。这个做法能有效避免CAR-T治疗导致的排异反应,但也让CAR-T疗法在治疗T细胞肿瘤时面临一个极大的风险:CAR-T可能被癌细胞污染。
事实上,在用CAR-T疗法治疗B细胞肿瘤时,就出现过癌细胞意外获得CAR,最终导致肿瘤失控的现象[2]。其原因很可能就是从患者体内分离获取的T细胞中,混入了极少量的恶性B细胞。
获得CAR的恶性B细胞,由于自体CAR和CD19的结合,还会对CD19靶向的CAR-T疗法耐药
如果用传统的自体CAR-T疗法治疗T细胞肿瘤,从患者体内充满恶性T细胞的血液中分离获取正常的T细胞,难度将会更高,更有可能混入恶性T细胞。因此,异体CAR-T或许是治疗T细胞肿瘤的最佳方法。
WU-CART-007正是一种异体CAR-T疗法,靶向95%以上T细胞淋巴瘤/白血病中都高表达的CD7分子,同时敲除了自身的CD7和T细胞受体(TCR),以避免自相残杀和排异反应。
WU-CART-007靶向CD7,并敲除了自身的CD7和TCR
本次研究一共纳入23位可评估患者,其中前12位患者为剂量扩展阶段,采用1亿细胞、3亿细胞、6亿细胞和9亿细胞四种不同剂量的WU-CART-007治疗,最终确定最佳的II期推荐方案为强化淋巴清除化疗后9亿细胞WU-CART-007治疗。后11位患者采用的正是这一方案。
全部23位患者中,12位患者在治疗后达到完全缓解,3位患者部分缓解,客观缓解率和完全缓解率分别达到65.2%和52.2%。这12位完全缓解的患者中,还有10人进行了微小残留病(MRD)的检测,7人检测结果为阴性。
WU-CART-007的疗效
特别是接受II期推荐方案的11位患者,8人完全缓解,2人部分缓解,客观缓解率和完全缓解率分别达到了90.9%和72.7%。
除了对肿瘤的控制外,针对T细胞肿瘤的CAR-T疗法还需特别关注对正常T细胞的影响,毕竟正常T细胞的缺失将会导致严重的免疫缺陷。
研究发现,接受WU-CART-007治疗的患者体内,随着WU-CART-007的扩增,CD7+正常T细胞数量快速下降直至消失,但同时出现了一群CD7-正常T细胞,不会造成持久的T细胞缺乏。
目前,WU-CART-007的后续临床试验已经启动,将在更多患者中进一步验证WU-CART-007的疗效和安全性。期待WU-CART-007能成为T细胞淋巴瘤患者的治疗新选择,也期待异体CAR-T技术能让CAR-T疗法降价,惠及更多患者。
参考文献:
[1]. Ghobadi A, Aldoss I, Maude S L, et al. Phase 1/2 Trial of Anti-CD7 Allogeneic WU-CART-007 in patients with Relapsed/Refractory T-cell Malignancies[J]. Blood, 2025.
[2]. Ruella M, Xu J, Barrett D M, et al. Induction of resistance to chimeric antigen receptor T cell therapy by transduction of a single leukemic B cell[J]. Nature medicine, 2018, 24(10): 1499-1503.
本文仅供医学药学专业人士阅读














 X
X