虽然免疫检查点抑制剂在HCC中取得了良好的效果,但免疫治疗在HCC中的应用仍面临许多挑战,如这类治疗的特点是应答率相对较低,缺乏肿瘤生物标志物来识别治疗敏感患者。图像引导的肿瘤消融(射频、微波或冷冻消融)已经应用于许多癌症,包括肾细胞癌、前列腺癌、肺癌和肝癌,并有很好的短期结果。然而,与射频消融和其他热消融方法相比,冷冻消融有几个相对优势,包括能够产生更大、更精确的消融区域,更清晰可识别的治疗区域,以及刺激免疫调节产生异位肿瘤抑制作用的能力。
在这里,我们给大家分享了一例因肿瘤破裂和出血诊断为HCC的患者,在术后肿瘤复发后采用抗血管生成和免疫治疗结合肿瘤内冷冻消融治疗后,持续的生存获益。
冷冻消融更有利,
联合治疗7个月达CR,
PFS超2年
患者男性,38岁,于2019年3月因严重腹痛就诊。患者有慢性乙型病毒性肝炎(HBV)病史,既往无抗病毒治疗。他的母亲和弟弟也有慢性乙型肝炎的病史。患者没有癌症家族史。
计算机断层扫描(CT)显示该患者在肝脏右下叶有一个破裂的肝脏肿瘤,并出现出血。该患者于2019年3月接受了紧急肝肿瘤切除术。术后病理诊断为肝细胞癌,血管内有肿瘤血栓。术后1个月行肝动脉造影,未见肝脏肿瘤染色。正电子发射断层扫描(PET-CT)显示肝右下叶肿瘤切除后无系统性转移。
2019年8月26日,患者行常规随访,上腹部增强磁共振成像(MRI)检查,发现肝脏多发转移瘤,较大病灶约6.3×4.3×4.7 cm,肝门淋巴结转移。提示患者巴塞罗那临床肝癌(BCLC)分期为C期。此时,患者甲胎蛋白(AFP)为6050 ng/mL。
随后,患者接受了肝脏肿瘤穿刺活检,并在美国病理学家学院认可的实验室对穿刺样本进行了NGS测序。检测结果显示患者程序细胞死亡配体1 (PD-L1)表达阴性,微卫星状态为MS-Stable,肿瘤突变负荷(TMB)为3 Muts/Mb。
患者随后开始接受仑伐替尼(12 mg/天)联合替吉奥胶囊(60mg,每日两次)治疗,但他出现了严重的恶心和呕吐。2019年9月初,患者甲胎蛋白(AFP)水平为90421.42 ng/mL。考虑到恶心呕吐可能主要由替吉奥胶囊引起,建议患者停止服用胶囊,但继续小剂量仑伐替尼 (8mg /天)治疗。
9月5日,我们在CT引导下对患者肝脏的一个大型转移性肿瘤进行了肿瘤内冷冻消融(其他病变和淋巴结未接受冷冻消融)。术后CT扫描显示肿瘤完全消融。在冷冻消融后的第4天,我们对未接受冷冻消融的转移性肝肿瘤进行CT引导下穿刺活检,并对组织样本和外周血浆进行NGS检测。NGS测序结果显示PD-L1表达阴性,MS-Stable微卫星状态,TMB为18.67 Muts/Mb。
9月11日,患者开始接受仑伐替尼(8 mg/天)联合免疫检查点抑制剂特瑞普利单抗(每3周静脉滴注240 mg)治疗,这是一种针对程序性细胞死亡1 (PD-1)受体的人源单克隆抗体。
10月8日,患者AFP降至5025.00 ng/mL。上腹部MRI提示,肝肿瘤综合治疗后,肝脏内可见多发肿块。考虑到肿瘤的部分存活,肿瘤坏死较前一张图像更为明显。

受这些额外结果的鼓舞,决定继续给予仑伐替尼联合特瑞普利单抗全身治疗。2019年12月初,患者的AFP水平降至17.20 ng/mL。上腹部MRI示肝脏多发异常信号及部分异常强化。考虑到大部分肿瘤坏死和部分存活,与之前在2019-10-09拍摄的图像相比,肿瘤体积减小。
此后,患者继续接受联合治疗。2020年4月的上腹部MRI显示肿瘤坏死,肿瘤体积继续缩小。根据mRECIST标准评估,患者已达到完全缓解(CR)。为了评估患者肝脏肿瘤残留活动性组织的程度,在B超引导下对疑似活动性肿瘤进行穿刺活检。穿刺活检标本的病理评估显示局部肝细胞增生伴水肿变性,部分区域纤维组织增生,未发现明显的恶性肿瘤。

患者持续联合治疗至今(最后一次治疗日期为2021年7月11日),常规检查中AFP水平始终低于正常值(0-7 ng/mL)。2021年8月PET-CT检查发现肝脏多发结节,FDG代谢降低,提示肝脏无肿瘤活动,全身无肿瘤转移,最后一次随访时的无进展生存期为24个月。整个治疗期间,患者无明显不适,无抗血管新生治疗或免疫治疗相关不良事件发生,HBV复制水平控制良好。
病例讨论
一例转移性肝癌患者,手术后疾病复发,然后接受冷冻消融,然后联合特瑞普利单抗和仑伐替尼。患者在治疗7个月后获得完全缓解,一直持续到提交本手稿,最后一次计算无进展生存期为24个月。
通过对肿瘤微环境的调控,提高肿瘤的治疗效果,是目前研究的热点。特别是大量研究表明,抗血管生成治疗联合免疫治疗可以使肿瘤血管正常,从而缓解肿瘤微环境的缺血缺氧,增加药物递送和抗肿瘤免疫细胞,并将肿瘤免疫抑制微环境转化为免疫支持微环境。基于这一理论,现在已有“T+A”和“双达”方案获批肝癌一线治疗。
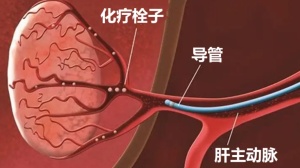
冷冻消融是一种局部治疗肿瘤病变的方法,常用于HCC患者。研究表明,与射频消融和微波消融相比,冷冻消融是安全的,显著改善了HCCs直径>2 cm的局部控制。更重要的是,冷冻消融可以产生一种外腔效应,这种效应被认为会影响原消融区以外的癌细胞。目前已有关于冷冻消融对免疫系统激活的作用的初步研究,但冷冻消融对肿瘤血管的作用的描述较少。有研究发现,冷冻消融后肿瘤组织中血管内皮生长因子(VEGF)的表达上调,残余肿瘤的血管新生明显增加。抗血管生成治疗可下调VEGF的表达,抑制肿瘤血管生成,从而提高冷冻消融对肿瘤的抑制作用。因此抗血管生成治疗联合冷冻消融也可能具有协同作用。但其协同治疗的机制尚不清楚,对药物剂量的选择、给药顺序、冷冻消融时间点也没有明确的标准,值得进一步研究。
参考来源:
Case Report: Antiangiogenic Therapy Plus Immune Checkpoint Inhibitors Combined With Intratumoral Cryoablation for Hepatocellular Carcinoma
本文仅供医学药学专业人士阅读





.jpg-pd13)










 X
X