老年多发肿瘤患者免疫治疗后高热并影像学病灶增大,到底该怎样鉴别?如何诊断?做何处理?金陵肺癌MDT论坛为您答疑解惑。
病例情况
2020年6-7月
行肺结节病灶伽马刀,剂量30Gy/15F。
2021-3-25
胸腹CT:右肺下叶病灶较前明显进展。
2021年4月
2021-4-26
首次来到解放军总医院第二医学中心就诊。
2021-5-17
完善肝穿刺活检,病理结果显示非霍奇金淋巴瘤,DLBCL非GCB型IV期B IPI4分。
2021-5-27至11-10
2021-8-19
2021-11-8
肺穿刺活检病理:肺浸润性粘液性腺癌(肠型);免疫组化:TIF-1(灶+),NapsinA(灶+),Alk-,CDX2+,Villil+,PD-L1(TPS<1%)。分子病理检测结果示CD74-NRG1融合突变。非霍奇金淋巴结化疗完成后暂时出院,2022年1月再次入院。
2022-1-11
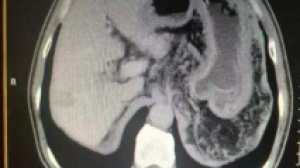
PET-CT:与2021-8-17检查比较:1.右肺下叶脊柱旁病变较前增大,代谢较前增高,考虑肺部病变较前进展(长径72mm,SUVmax12.8 vs 8.0);2.双肺门淋巴结代谢较前增高,考虑反应性改变可能性大;右侧胸膜增厚;3.肝右叶两处略低密度区较前相仿,肝内未见异常高代谢征象。
2022-1-21
行第一周期帕博利珠单抗治疗。
2022-2-5
(C1D15):开始发热,体温>38℃(38-39℃),轻度畏寒、寒战,无咳嗽、咳痰,无腹痛,无尿频、尿痛等症状。完善血常规:CRP 11mg/dl,白细胞5.9*10^9/L,中性粒0.783,内毒素测定(-),PCT正常。血培养阴性。肺部CT:右下肺基底段实性团块影,较2021-11-18、2022-1-15对比,逐渐增大,未见感染灶。
2022-2-10
血常规:CRP 10.09mg/dl、白细胞4.21*10^9/L,中性粒0.587,血培养阴性。
2022-2-11
2022-2-17
2022-2-18
封面图
2022-2-25:肺部CT:右下肺基底段实性团块影,与2021-11-18、2022-12-5、2022-2-15比逐渐增大,符合考虑恶性肿瘤,右肺外基底段结节影较2022-2-5比稍增大,转移不除外。
2022-3-15
第一周期白蛋白结合型紫杉醇100mg;
2022-2-5
2022-5-17
2022-6-8
2022-6-8
肺部CT:右肺下叶病灶较前缩小。
本文仅供医学药学专业人士阅读











 X
X