“厉害了,双免疫联合疗法,有效率42%,包括9%患者肿瘤完全消失,美国FDA火速批准上市!”
作为这几年肿瘤治疗领域最大的突破,PD-1抗体堪称“抗癌神药”,彻底改变了肿瘤治疗的格局。其优势在于:
一旦起效,患者可能实现长期生存5-10年,这是最吸人的地方,让我们看到了治愈肿瘤的希望;同时,PD-1针对多种肿瘤都有效果,包括肝癌、肺癌、胃癌、肾癌和黑色素瘤等。
不过,PD-1也有自己的问题:单药有效率不高,针对大部分肿瘤有效率只有20%左右。
所以,全世界的科学家和临床医生都在研究同一个问题:如何提高PD-1抗体的有效率?为更多的患者争取这来之不易的治愈良机。其中,联合治疗是一个选择,比如PD-1联合放疗、化疗和靶向药等,有效率可以大幅度提高。
上周,PD-1治疗领域再传捷报:美国FDA(食品药品监督管理局)批准了新的免疫联合疗法上市,临床数据显示:
针对预后差的晚期肾癌患者:直接使用双免疫联合疗法(PD-1+CTLA-4),有效率高达42%(ORR),包括9%的患者肿瘤消失(CR);而用传统靶向药舒尼替尼的有效率只有27%,1%的患者肿瘤消失。
高下立判,双免疫联合疗法实力碾压传统治疗,再次改写肾癌治疗格局。
FDA是根据一个代号为CheckMate – 214的临床试验数据批准的这个适应症。CheckMate – 214是一个全球多中心的大型三期临床试验,从2014年10月在全球招募患者,到2017年6月结束,试验的目的就是比较在晚期肾癌患者中,使用新的治疗药物PD-1抗体联合CTLA-4抗体是不是比传统的老药-舒尼替尼效果更好。
临床设计:
招募大约1000位晚期肾癌患者,分成两组,一组(425位)使用PD-1抗体Opdivo(3mg/kg)联合CTLA-4抗体Yervoy(1mg/kg),三周一次,联合四次之后,单药Opdivp(3mg/kg),两周一次;另外一组(422人)使用舒尼替尼,每天口服50mg,用4周停2周。
临床数据:
在有效率方面,联合治疗组有177位患者肿瘤缩小至少30%,达到PR标准,客观有效率42%;而舒尼替尼组只有114位患者肿瘤达到PR标准,客观有效率只有27%。更重要的是,联合用药组有9%的患者肿瘤完全消失,而舒尼替尼组只有1%的患者肿瘤消失。所以,联合用药组的有效率提高了近50%。具体如下:

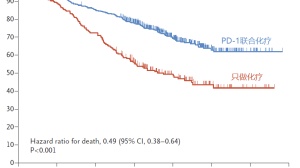
在生存期方面,评价一个新药是不是比老药最好的金标准就是看谁能让患者活的更长,联合治疗组患者的12个月生存率是80%,18个月生存率是75%,而舒尼替尼组2个月生存率是72%,18个月生存率是60%。很明显,联合用药组的患者活的更长,具体如下:

在副作用方面,联合用药组患者发生3-4级比较严重副作用的比例是46%。而舒尼替尼组的比例高达63%,所以,看起来联合治疗组的副作用更小。
所以,对于预后较差的晚期肾癌患者来说,双免疫联合疗法的有效率更高、肿瘤消失的比例更高、生存期更长、副作用也更小,完爆老药舒尼替尼。
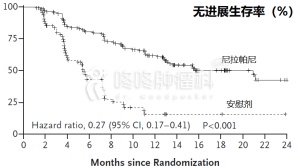
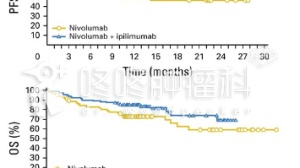
其实,早在2015和2016年,基于一个二期和三期临床数据Checkmate 067和0692,FDA就批准了PD-1抗体Opdivo联合CTLA-4抗体Yervoy用于晚期恶性黑色素瘤:相比于单药Opdivo,联合治疗组的有效率超过50%,无进展生存期也明显延长11.5个月 VS 6.9个月,具体如下图:

不过,针对恶黑的联合治疗方案不同于上面的肾癌,Opdivo的剂量是1mg/kg,Yervoy的剂量是3mg/kg,副作用巨大,很多患者扛不住副作用,不得已退出临床试验,建议国内的患者进行联合治疗的时候可以参考肾癌的剂量。
到目前为止,在免疫联合治疗的探索上,依然只有PD-1联合CTLA-4抗体和化疗得到了FDA的认可,分别被批准用于恶黑和肺癌的一线治疗。接下来,我们还有更多期待,包括靶向药仑伐替尼(E7080)、阿昔替尼,细胞因子药物(NKTR-214)等,详情参考:
参考文献:
[1] Motzer, R. J. et al. Nivolumab plus Ipilimumab versus Sunitinib in Advanced Renal-Cell Carcinoma. N Engl J Med, doi:10.1056/NEJMoa1712126 (2018).
[2] Larkin, J. et al. Combined Nivolumab and Ipilimumab or Monotherapy in Untreated Melanoma. N Engl
[3] https://www.onclive.com/web-exclusives/fda-approves-nivolumabipilimumab-for-frontline-rcc
本文仅供医学药学专业人士阅读
















 X
X